高中原电池知识点总结
时间:2021-08-31原电池是高一化学课本中的重要知识,同学们一定要牢记。下面是小编为你收集整理的高一化学原电池的知识点归纳,一起来看看吧。
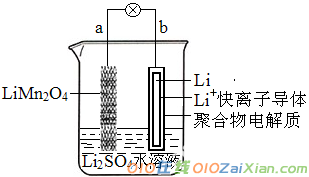
高一化学原电池知识点
一、原电池、电解池的两极
电子从负极通过导线流向正极,电子的定向移动形成电流,电流的方向是正极到负极,这是物理学规定的。
阴极、阳极是电化学规定的,失去电子的极即氧化极,也就是阳极;得到电子的极即还原极,也就是阴极。
原电池中阳极失去电子,电子由阳极通过导线流向阴极,阴极处发生得电子的反应,由于原电池是一种化学能转化为电能的装置,它作为电源,通常我们称其为负极和正极。在电解池中,连着负极的一极是电解池的阴极,连着正极的一极是电解池的阳极,由于电解池是一种电能转化为化学能的装置,我们通常说明它的阳极和阴极。
二、原电池、电解池、电镀池的判断规律
(1)若无外接电源,又具备组成原电池的三个条件。①有活泼性不同的两个电极;②两极用导线互相连接成直接插入连通的电解质溶液里;③较活泼金属与电解质溶液能发生氧化还原反应(有时是与水电离产生的H+作用),只要同时具备这三个条件即为原电池。
(2)若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池;当阴极为金属,阳极亦为金属且与电解质溶液中的金属离子属同种元素时,则为电镀池。
(3)若多个单池相互串联,又有外接电源时,则与电源相连接的装置为电解池成电镀池。若无外接电源时,先选较活泼金属电极为原电池的负极(电子输出极),有关装置为原电池,其余为电镀池或电解池。
随机推荐
上一篇:高一生物备课组总结
下一篇:高中一年级化学知识点总结











